Rak jelita grubego to jeden z najczęstszych nowotworów złośliwych w Polsce i na świecie, stanowiąc istotny problem zdrowia publicznego. Według danych Krajowego Rejestru Nowotworów każdego roku w Polsce odnotowuje się około 18–20 tysięcy nowych zachorowań na raka jelita grubego, a liczba zgonów przekracza 10 tysięcy rocznie. Umiejscawia to więc raka jelita grubego w ścisłej czołówce przyczyn zgonów onkologicznych – obok takich chorób jak rak płuca, rak piersi czy rak gruczołu krokowego.
Nowotwory jelita grubego rozwijają się w dowolnej jego części, to znaczy w okrężnicy lub odbytnicy (Rycina 1). Z perspektywy klinicznej szczególnie istotne jest to, że rak jelita grubego rozwija się powoli i przez długi czas może nie dawać wyraźnych objawów klinicznych. W wielu przypadkach pierwsze objawy, takie jak obecność krwi w kale, zmiana rytmu wypróżnień czy niedokrwistość, pojawiają się dopiero w bardziej zaawansowanym stadium choroby. Tymczasem dane epidemiologiczne pokazują, że wczesne wykrycie znacząco poprawia rokowanie i zwiększa szanse na całkowite wyleczenie. Dlatego tak ogromne znaczenie ma znajomość czynników ryzyka oraz świadome uczestnictwo w programach badań przesiewowych.
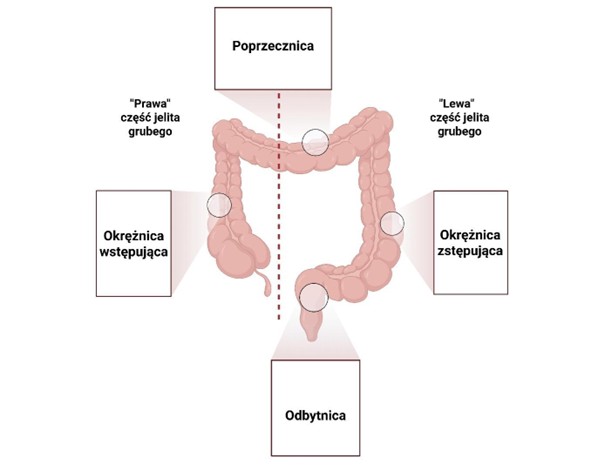
Rycina 1. Schemat anatomiczny jelita grubego.
Kluczową informacją dla pacjentów jest fakt, że około 85–90% przypadków raka jelita grubego rozwija się na podłożu łagodnych zmian, jakimi są polipy, najczęściej gruczolaki. Te niewielkie zmiany w obrębie błony śluzowej jelita grubego mogą przez wiele lat pozostawać bezobjawowe, jednak w wyniku nagromadzenia mutacji genetycznych mogą przekształcić się w nowotwór złośliwy. Co istotne, polipy można skutecznie wykryć i usunąć podczas badania kolonoskopowego, które pozostaje złotym standardem w diagnostyce nowotworów jelita grubego. Pozwala to przerwać proces rozwoju raka jeszcze na etapie przedinwazyjnym.
Zrozumienie, czym jest rak jelita grubego, jakie są główne przyczyny raka jelita grubego oraz które czynniki ryzyka można modyfikować, stanowi fundament skutecznej profilaktyki. W obliczu rosnącej liczby zachorowań na raka jelita grubego w starzejącym się społeczeństwie działania prewencyjne mają realny wpływ na zdrowie populacji. W dalszej części artykułu szczegółowo omówione zostaną wszystkie istotne czynniki ryzyka – zarówno genetyczne, jak i środowiskowe – oraz aktualne zalecenia dotyczące profilaktyki raka jelita grubego i badań przesiewowych.
1. Epidemiologia raka jelita grubego w Polsce i na świecie:
Rak jelita grubego jest jednym z najczęściej diagnozowanych nowotworów na świecie. Według danych World Health Organization oraz projektu GLOBOCAN w 2020 roku odnotowano ponad 1,9 miliona nowych przypadków tego nowotworu oraz około 930 tysięcy zgonów rocznie. Oznacza to, że nowotwór jelita grubego zajmuje trzecie miejsce pod względem zachorowalności i drugie pod względem umieralności wśród wszystkich nowotworów złośliwych globalnie. W Polsce sytuacja epidemiologiczna jest równie poważna. Z danych Krajowego Rejestru Nowotworów wynika, że rak jelita grubego jest drugim najczęściej występującym nowotworem złośliwym w populacji ogólnej, a wśród przyczyn zgonów onkologicznych plasuje się w ścisłej czołówce. Każdego roku notuje się około 18–20 tysięcy nowych zachorowań na raka jelita grubego, a liczba zgonów przekracza 10 tysięcy. Wskaźniki zachorowalności są wyższe u mężczyzn niż u kobiet, jednak różnice te stopniowo się zmniejszają. Analiza trendów pokazuje, że zachorowania na raka jelita grubego rosną szczególnie w krajach wysoko rozwiniętych. Zjawisko to wiąże się z tzw. „zachodnim stylem życia”, obejmującym dietę bogatą w czerwone i przetworzone mięso, niską aktywność fizyczną, otyłość, palenie tytoniu oraz spożycie alkoholu. Czynniki te zwiększają ryzyko rozwoju raka jelita grubego poprzez przewlekły stan zapalny, zaburzenia mikrobioty jelitowej oraz niekorzystne zmiany metaboliczne. Jednocześnie w części państw obserwuje się stabilizację lub nawet spadek umieralności, co jest efektem skuteczniejszych programów badań przesiewowych i lepszej diagnostyki. Regularne wykonywanie takich badań jak kolonoskopia pozwala wykryć chorobę we wczesnych stadiach, kiedy rokowanie jest znacznie korzystniejsze.
Rak jelita grubego jest chorobą silnie związaną z wiekiem. Ryzyko zachorowania znacząco wzrasta po 50 roku życia, dlatego właśnie od tego wieku rozpoczynają się populacyjne badania przesiewowe w wielu krajach, w tym w Polsce. Szacuje się, że ponad 90% przypadków raka jelita grubego dotyczy osób powyżej 50 roku życia. Niepokojącym zjawiskiem ostatnich lat jest jednak rosnąca zachorowalność wśród osób młodszych, poniżej 50 roku życia. Przyczyny tego trendu nie są do końca poznane, ale podejrzewa się związek z otyłością, dietą ubogą w błonnik, spożyciem wysoko przetworzonej żywności oraz zaburzeniami mikrobioty jelitowej. Zjawisko to podkreśla znaczenie świadomości pierwszych objawów oraz konieczność indywidualnej oceny ryzyka zachorowania na raka jelita także u młodszych pacjentów.
Lokalizacja, w której rozwija się rak jelita grubego, ma istotne znaczenie kliniczne – wpływa na obraz objawów, sposób diagnostyki, wybór leczenia oraz rokowanie. W praktyce klinicznej wyróżnia się nowotwory prawej części jelita (jelito ślepe, okrężnica wstępująca, proksymalna część poprzecznicy) oraz lewej części jelita (dystalna poprzecznica, okrężnica zstępująca, esica, odbytnica). Różnice wynikają zarówno z budowy anatomicznej, jak i odmiennych mechanizmów molekularnych rozwoju nowotworu. Guzy zlokalizowane w prawej części jelita grubego rosną w odcinku o większym świetle i bardziej płynnej treści jelitowej. Z tego powodu przez długi czas nie powodują objawów mechanicznych. Często rozwijają się podstępnie i są rozpoznawane w bardziej zaawansowanym stadium. Charakterystyczne objawy dla guzów zlokalizowanych w prawej części jelita to przewlekła utrata krwi z przewodu pokarmowego (często utajona), niedokrwistość z niedoboru żelaza i związane z nią osłabienie, męczliwość, utrata masy ciała, oraz dyskomfort lub tępy ból w prawej połowie jamy brzusznej. W tych przypadkach krwawienie z przewodu pokarmowego ma zwykle charakter przewlekły i niewidoczny gołym okiem. Pacjent nie obserwuje świeżej krwi w kale, a pierwszym objawem bywa niedokrwistość wykryta w badaniach laboratoryjnych. Pod względem biologicznym nowotwory prawej strony częściej wykazują niestabilność mikrosatelitarną (MSI) i są związane z mutacjami określonych genów. Nowotwory lewej strony jelita rozwijają się w odcinku o mniejszym świetle, gdzie treść jelitowa jest bardziej uformowana. Nawet stosunkowo niewielki guz może więc prowadzić do objawów zwężenia światła jelita. Charakterystyczne objawy obejmują zwykle zmianę rytmu wypróżnień (naprzemienne zaparcia i biegunki), uczucie niepełnego wypróżnienia, widoczną świeżą krew w kale, objawy niedrożności jelit (wzdęcia, zatrzymanie gazów i stolca). W przypadku nowotworów odbytnicy dodatkowo mogą występować parcie na stolec, śluz w kale. Ze względu na szybsze pojawienie się objawów mechanicznych nowotwory lewej strony są często rozpoznawane wcześniej niż guzy prawej części jelita. W stadium miejscowym ich rokowanie bywa korzystniejsze, ponieważ choroba rzadziej jest już rozsiana w chwili diagnozy. W stadium wczesnym (I–II) rokowanie jest dobre niezależnie od lokalizacji, a 5-letnie przeżycia przekraczają 80–90%. W stadium przerzutowym różnice między stroną prawą a lewą stają się bardziej widoczne – guzy lewej strony zwykle wiążą się z lepszym rokowaniem niż guzy prawej strony.
2. Czynniki genetyczne w rozwoju raka jelita grubego
Rozwój raka jelita grubego jest procesem wieloczynnikowym, w którym istotną rolę odgrywają uwarunkowania genetyczne. Szacuje się, że około 20–30% przypadków tego nowotworu ma związek z obciążeniem rodzinnym, natomiast 5–10% stanowią jasno określone dziedziczne zespoły predysponujące do zachorowania. Oznacza to, że u znacznej części pacjentów ryzyko zachorowania na raka jelita jest większe niż w populacji ogólnej ze względu na odziedziczone zmiany w materiale genetycznym.
Najważniejszym elementem oceny ryzyka pozostaje dokładny wywiad rodzinny. Obecność raka jelita grubego u krewnych pierwszego stopnia – rodziców, rodzeństwa lub dzieci – zwiększa ryzyko zachorowania od 2 do 4 razy. Ryzyko to rośnie wraz z liczbą chorych członków rodziny oraz w sytuacji, gdy nowotwór został rozpoznany w młodym wieku, zwłaszcza przed 50 rokiem życia. Im więcej przypadków raka jelita grubego w rodzinie i im wcześniej wystąpiły, tym większe prawdopodobieństwo, że w danej rodzinie występuje predyspozycja genetyczna wymagająca szczególnego nadzoru.
Do najlepiej poznanych dziedzicznych zespołów zwiększających ryzyko rozwoju raka jelita grubego należą zespół Lyncha oraz rodzinna polipowatość gruczolakowata. Zespół Lyncha jest związany z mutacjami genów odpowiedzialnych za naprawę uszkodzeń DNA. W efekcie komórki nabłonka jelita grubego nie są w stanie skutecznie eliminować błędów powstających podczas podziałów komórkowych, co sprzyja akumulacji mutacji i wczesnemu rozwojowi nowotworu. Osoby z tym zespołem mają zwiększone ryzyko nie tylko raka jelita grubego, ale również innych nowotworów, w tym raka trzonu macicy czy raka żołądka człowieka. Rodzinna polipowatość gruczolakowata jest rzadszą postacią dziedzicznej predyspozycji. W jej przebiegu, na skutek mutacji genu APC, w jelicie grubym rozwijają się liczne polipy gruczolakowe. W przypadku braku odpowiedniego leczenia niemal nieuchronnie dochodzi do transformacji tych zmian w nowotwór złośliwy, często jeszcze przed 40 rokiem życia. Przykład ten pokazuje, jak silny wpływ na rozwój raka jelita grubego może mieć pojedyncza mutacja genu o kluczowym znaczeniu dla kontroli podziałów komórkowych.
Warto jednak podkreślić, że nawet w przypadkach sporadycznych, czyli niezwiązanych z wyraźnym zespołem dziedzicznym, rozwój nowotworu jelita grubego jest konsekwencją nagromadzenia wielu zmian genetycznych w komórkach nabłonka jelita. Proces ten obejmuje stopniowe uszkadzanie genów odpowiedzialnych za kontrolę cyklu komórkowego, naprawę DNA oraz mechanizmy apoptozy, czyli zaprogramowanej śmierci komórki. W efekcie komórki zaczynają dzielić się w sposób niekontrolowany, tracą zdolność do prawidłowej regulacji wzrostu i tworzą guz nowotworowy, który z czasem może naciekać okoliczne tkanki i dawać przerzuty. Genetyka odgrywa zatem kluczową rolę w rozwoju raka jelita grubego, jednak sama predyspozycja nie oznacza nieuchronności choroby. Wczesna identyfikacja osób z grupy podwyższonego ryzyka, konsultacja genetyczna oraz odpowiednio wcześnie wdrożone badania przesiewowe, takie jak kolonoskopia, pozwalają znacząco zmniejszyć ryzyko rozwoju zaawansowanego nowotworu jelita grubego i poprawić rokowanie.
2.1 Zespół Lyncha i rodzinna polipowatość gruczolakowata
Dziedziczne zespoły predysponujące do raka jelita grubego odpowiadają za około 5–10% wszystkich zachorowań, ale w tej grupie pacjentów ryzyko rozwoju nowotworu jest wielokrotnie wyższe niż w populacji ogólnej i ujawnia się w młodszym wieku. Najważniejszymi klinicznie zespołami są Zespół Lyncha oraz Rodzinna polipowatość gruczolakowata, które różnią się mechanizmem molekularnym, przebiegiem oraz zasadami nadzoru onkologicznego.
Zespół Lyncha (dziedziczny rak jelita grubego niezwiązany z polipowatością) jest spowodowany mutacjami w genach systemu naprawy DNA (MLH1, MSH2, MSH6, PMS2). Uszkodzenie mechanizmów naprawczych prowadzi do niestabilności mikrosatelitarnej i przyspieszonego gromadzenia mutacji w komórkach nabłonka jelita. Ryzyko zachorowania na raka jelita grubego w ciągu życia wynosi 60–80%, a średni wiek rozpoznania to około 45 lat, czyli znacznie wcześniej niż w populacji ogólnej. Nowotwory te często lokalizują się w prawej części jelita grubego i mogą rozwijać się szybko, bez długiej fazy obecności licznych polipów.
Zgodnie z aktualnymi wytycznymi (m.in. NCCN, ESMO), nadzór onkologiczny u osób z zespołem Lyncha obejmuje rozpoczęcie kolonoskopii w wieku 20–25 lat lub 2–5 lat wcześniej niż najwcześniejsze zachorowanie w rodzinie. Badanie powinno być powtarzane co 1–2 lata. Zaleca się również monitorowanie pod kątem innych nowotworów, zwłaszcza raka endometrium i raka żołądka człowieka, a w wybranych przypadkach rozważa się profilaktyczne zabiegi chirurgiczne. Intensywny nadzór pozwala na wykrycie zmian w bardzo wczesnych stadiach, co znacząco poprawia rokowanie.
Odmienny przebieg ma rodzinna polipowatość gruczolakowata (FAP), związana z mutacją genu APC. Choroba ta prowadzi do rozwoju setek lub tysięcy polipów w obrębie jelita grubego już w okresie dojrzewania. Każdy z tych polipów może ulec transformacji w nowotwór złośliwy, dlatego bez leczenia niemal 100% pacjentów rozwinie raka jelita grubego przed 40. rokiem życia. W przeciwieństwie do zespołu Lyncha, w FAP proces nowotworzenia przebiega przez klasyczną sekwencję gruczolak–rak, ale ze względu na ogromną liczbę polipów ryzyko jest praktycznie nieuniknione.
Wytyczne zalecają rozpoczęcie badań endoskopowych (rektosigmoidoskopia lub kolonoskopia) już w wieku 10–12 lat u osób z podejrzeniem FAP. Badania powinny być wykonywane corocznie. Po potwierdzeniu licznych polipów standardem postępowania jest profilaktyczna kolektomia, czyli chirurgiczne usunięcie jelita grubego, zwykle między 16. a 25. rokiem życia, zanim dojdzie do rozwoju raka. Pacjenci wymagają również dalszego nadzoru pooperacyjnego oraz kontroli górnego odcinka przewodu pokarmowego ze względu na ryzyko innych nowotworów.
Wśród rzadszych zespołów genetycznych należy wymienić zespół Peutza-Jeghersa oraz polipowatość młodzieńczą. Charakteryzują się one obecnością mnogich polipów hamartomatycznych oraz zwiększonym ryzykiem nowotworów przewodu pokarmowego i innych narządów. Również w tych przypadkach obowiązuje indywidualnie dobrany program badań przesiewowych rozpoczynanych w młodym wieku.
Dziedziczne zespoły nowotworowe pokazują, że w określonych sytuacjach ryzyko zachorowania na raka jelita grubego jest ekstremalnie wysokie i wymaga zupełnie innej strategii postępowania niż w populacji ogólnej. Wczesna diagnostyka genetyczna, regularna kolonoskopia oraz – w wybranych przypadkach – leczenie chirurgiczne o charakterze profilaktycznym pozwalają znacząco zmniejszyć ryzyko rozwoju zaawansowanego nowotworu jelita grubego i poprawić długoterminowe rokowanie.
3. Czynniki dietetyczne zwiększające ryzyko zachorowania na raka jelita grubego
Dieta jest jednym z najważniejszych modyfikowalnych czynników ryzyka rozwoju raka jelita grubego. Liczne badania populacyjne i metaanalizy wskazują, że wzorzec żywieniowy charakterystyczny dla krajów uprzemysłowionych, określany jako „zachodni”, wiąże się z wyższą częstością zachorowań na nowotwór jelita grubego. Model ten obejmuje wysokie spożycie żywności wysoko przetworzonej, czerwonego i przetworzonego mięsa, tłuszczów nasyconych oraz cukrów prostych, przy jednoczesnym niedoborze błonnika, warzyw i produktów pełnoziarnistych.
Szczególną uwagę zwraca rosnące spożycie produktów ultraprzetworzonych, czyli żywności poddanej wieloetapowej obróbce technologicznej i zawierającej dodatki takie jak emulgatory, stabilizatory, konserwanty czy wzmacniacze smaku. Badania kohortowe obejmujące setki tysięcy osób wykazały, że wysokie spożycie tego typu produktów wiąże się z wyraźnym wzrostem ryzyka rozwoju raka jelita grubego, zwłaszcza w dystalnych odcinkach jelita. Do grup szczególnie niekorzystnych należą gotowe wyroby mięsne, dania typu fast food, słodkie napoje gazowane oraz pakowane przekąski o wysokiej zawartości soli i tłuszczu. Produkty te są zazwyczaj ubogie w składniki ochronne, a jednocześnie sprzyjają nadmiernej podaży energii i przyrostowi masy ciała.
Istotnym elementem diety zwiększającym ryzyko zachorowania na raka jelita grubego jest również regularne spożywanie czerwonego mięsa oraz mięsa przetworzonego. World Health Organization uznała przetworzone mięso za czynnik rakotwórczy dla człowieka, a czerwone mięso za prawdopodobnie rakotwórcze. Związek ten potwierdzono w licznych analizach epidemiologicznych, w których obserwowano wzrost ryzyka wraz z ilością i częstotliwością spożycia. Mechanizmy biologiczne obejmują między innymi działanie hemu obecnego w czerwonym mięsie, powstawanie N-nitrozozwiązków podczas przetwarzania oraz tworzenie związków mutagennych w trakcie obróbki w wysokiej temperaturze, takich jak heterocykliczne aminy aromatyczne. Długotrwała ekspozycja na te substancje może prowadzić do uszkodzeń DNA komórek nabłonka jelita grubego i inicjować proces karcynogenezy.
Dieta wysokotłuszczowa i wysokokaloryczna, szczególnie bogata w tłuszcze nasycone oraz produkty zawierające duże ilości cukrów prostych, sprzyja rozwojowi nadwagi i otyłości, które same w sobie stanowią istotny czynnik ryzyka raka jelita grubego. Otyłość wiąże się z przewlekłym stanem zapalnym, zaburzeniami hormonalnymi oraz podwyższonym stężeniem insuliny i insulinopodobnego czynnika wzrostu. Te czynniki mogą pobudzać podziały komórek nabłonka jelita i sprzyjać rozwojowi nowotworu. Nadmiar tłuszczów wpływa również na metabolizm kwasów żółciowych, prowadząc do powstawania wtórnych kwasów żółciowych o działaniu drażniącym i potencjalnie rakotwórczym dla błony śluzowej jelita.
Nieprawidłowa dieta oddziałuje także na mikrobiotę jelitową. Niski udział błonnika i wysoka zawartość przetworzonych produktów mogą prowadzić do zmniejszenia liczby korzystnych bakterii produkujących krótkołańcuchowe kwasy tłuszczowe, które mają działanie przeciwzapalne i ochronne wobec nabłonka jelita. Zaburzenia równowagi mikrobiologicznej sprzyjają natomiast utrzymywaniu się przewlekłego stanu zapalnego, zwiększonej przepuszczalności bariery jelitowej oraz większej podatności komórek na uszkodzenia genetyczne.
Ważnym czynnikiem dietetycznym zwiększającym ryzyko zachorowania na raka jelita grubego jest również alkohol. Etanol metabolizowany jest do aldehydu octowego, związku o udowodnionym działaniu rakotwórczym, który może uszkadzać DNA i zaburzać procesy naprawcze w komórkach. Badania epidemiologiczne wskazują, że nawet umiarkowane spożycie alkoholu wiąże się ze wzrostem ryzyka zachorowania, a ryzyko to zwiększa się wraz z ilością spożywanego etanolu. Alkohol może ponadto nasilać stres oksydacyjny oraz zaburzać wchłanianie niektórych witamin o potencjalnym działaniu ochronnym.
Zgromadzone dane naukowe jednoznacznie pokazują, że sposób żywienia ma realny wpływ na ryzyko rozwoju raka jelita grubego. Dieta bogata w żywność wysoko przetworzoną, tłuszcze nasycone, cukry proste i alkohol sprzyja mechanizmom biologicznym prowadzącym do karcynogenezy, podczas gdy zmiana nawyków żywieniowych stanowi jeden z najważniejszych elementów profilaktyki pierwotnej
3.1 Rola czerwonego mięsa i przetworzonych produktów
Związek między spożyciem czerwonego mięsa i przetworzonych produktów mięsnych a rakiem jelita grubego jest jednym z najlepiej udokumentowanych tematów w profilaktyce żywieniowej. World Health Organization / IARC klasyfikuje przetworzone mięso jako kancerogen grupy 1 (udowodnione działanie rakotwórcze), a czerwone mięso jako kancerogen grupy 2A (prawdopodobnie rakotwórcze).
W przypadku czerwonego mięsa istotną rolę odgrywa obecność hemu, który może nasilać stres oksydacyjny w świetle jelita i indukować peroksydację lipidów. W jej przebiegu powstają reaktywne produkty, m.in. aldehyd malonowy, które mogą uszkadzać DNA komórek nabłonka i sprzyjać powstawaniu mutacji. Równolegle podczas trawienia i w warunkach jelitowych może dochodzić do zwiększonego tworzenia związków N-nitrozowych, które mają potencjał genotoksyczny.
W mięsie przetworzonym dodatkowym źródłem ryzyka są procesy peklowania i konserwacji z użyciem azotynów i azotanów. W przewodzie pokarmowym mogą one uczestniczyć w reakcji prowadzącej do powstawania związków N-nitrozowych, a długotrwała ekspozycja może sprzyjać karcynogenezie.
Znaczenie ma również sposób przygotowania mięsa. Smażenie i grillowanie w wysokiej temperaturze sprzyjają powstawaniu heterocyklicznych amin aromatycznych i wielopierścieniowych węglowodorów aromatycznych, które wykazują działanie mutagenne w badaniach laboratoryjnych i są traktowane jako jeden z mechanizmów łączących „mocno przypieczone” mięso z ryzykiem nowotworu jelita grubego.
W praktyce profilaktycznej rekomenduje się ograniczanie ekspozycji: według zaleceń WCRF/AICR, jeśli jadasz czerwone mięso, warto utrzymywać spożycie na poziomie nie większym niż około 350–500 g masy po obróbce tygodniowo, a przetworzone mięso spożywać „jak najmniej, najlepiej wcale”.
4. Czynniki związane ze stylem życia
Czynniki związane ze stylem życia należą do najlepiej udokumentowanych, modyfikowalnych czynników ryzyka rozwoju raka jelita grubego. Duże badania kohortowe oraz metaanalizy konsekwentnie pokazują, że nadmierna masa ciała, niska aktywność fizyczna i palenie tytoniu zwiększają ryzyko zachorowania na nowotwór jelita grubego niezależnie od wieku czy wywiadu rodzinnego. W praktyce oznacza to, że nawet przy obecności czynników niemodyfikowalnych, poprawa stylu życia może realnie obniżać ryzyko rozwoju raka.
Najsilniej i najbardziej powtarzalnie wykazanymi czynnikami są nadwaga i otyłość, oceniane m.in. poprzez wskaźnik masy ciała (BMI) oraz miary otyłości brzusznej. Badania wskazują, że wraz ze wzrostem BMI rośnie ryzyko raka jelita grubego, przy czym zależność jest zwykle wyraźniejsza u mężczyzn, a miary tłuszczu trzewnego (np. obwód talii) mają istotne znaczenie; zależność ta, choć mniej nasilona, dotyczy także kobiet. W ujęciu biologicznym tkanka tłuszczowa działa jak aktywny narząd endokrynny i immunologiczny: produkuje cytokiny prozapalne (m.in. IL-6, TNF-α), adipokiny oraz mediatory stresu oksydacyjnego. Tworzy to przewlekły, niskonasilony stan zapalny, który sprzyja uszkodzeniom DNA, nasileniu proliferacji komórek oraz zaburzeniom nadzoru immunologicznego w obrębie jelita.
Drugim kluczowym mechanizmem łączącym otyłość z karcynogenezą jest zaburzenie osi metabolicznej insulina–IGF. Otyłości często towarzyszy insulinooporność i hiperinsulinemia, a podwyższone stężenie insuliny oraz insulinopodobnego czynnika wzrostu (IGF-1) aktywuje szlaki sygnałowe promujące wzrost komórek i hamujące apoptozę. W konsekwencji komórki nabłonka jelita z nabytymi zmianami genetycznymi mają większą szansę przetrwania i dalszej ekspansji. W otyłości obserwuje się też zmiany w metabolizmie kwasów żółciowych, a także w składzie mikrobioty jelitowej, co może sprzyjać produkcji metabolitów o działaniu prozapalnym i potencjalnie toksycznym oraz zwiększać przepuszczalność bariery jelitowej.
Niska aktywność fizyczna i siedzący tryb życia stanowią niezależne czynniki ryzyka. Metaanalizy wskazują, że osoby o wyższym poziomie aktywności fizycznej rzadziej chorują na raka okrężnicy, a efekt ochronny jest obserwowany w wielu populacjach i różnych typach aktywności. Równolegle analizy dotyczące zachowań sedentarnych pokazują, że długotrwałe siedzenie wiąże się ze wzrostem ryzyka, nawet gdy uwzględnia się inne elementy stylu życia. Z perspektywy mechanizmów biologicznych regularny wysiłek fizyczny obniża markery stanu zapalnego, poprawia wrażliwość na insulinę i zmniejsza stymulację osi insulina–IGF, a także wspiera odporność przeciwnowotworową (m.in. poprzez korzystny wpływ na funkcje komórek NK i równowagę cytokin). Dodatkowo przyspieszenie pasażu jelitowego skraca czas kontaktu błony śluzowej z potencjalnymi czynnikami rakotwórczymi w treści jelitowej, co ma znaczenie zwłaszcza przy współistniejących niekorzystnych nawykach dietetycznych.
Palenie tytoniu jest kolejnym dobrze potwierdzonym czynnikiem ryzyka. Wykazano, że osoby palące częściej rozwijają raka jelita grubego, a związek ten jest szczególnie widoczny przy długotrwałej ekspozycji. Co ważne klinicznie, palenie zwiększa także ryzyko powstawania polipów gruczolakowatych, czyli zmian prekursorowych, z których wywodzi się większość przypadków raka jelita grubego. Dym tytoniowy dostarcza związków rakotwórczych (m.in. nitrozoaminy i wielopierścieniowe węglowodory aromatyczne), które mogą docierać do jelita z krwią lub po połknięciu śliny i działać toksycznie, nasilając stres oksydacyjny oraz zaburzając naprawę DNA. Palenie wpływa też na mikrośrodowisko zapalne, co może ułatwiać progresję zmian od polipa do nowotworu.
Na marginesie głównych czynników coraz częściej omawia się także rolę przewlekłego stresu, zaburzeń snu i rytmu dobowego oraz niskiego poziomu witaminy D związanego z ograniczoną ekspozycją na słońce. W badaniach obserwacyjnych wyższe stężenia witaminy D częściej korelują z niższym ryzykiem raka jelita grubego, a biologicznie jest to spójne z udziałem witaminy D w kontroli różnicowania komórek, apoptozy i odpowiedzi immunologicznej. Zależności te są jednak bardziej złożone i w mniejszym stopniu „przekładalne” na proste zalecenia niż w przypadku redukcji masy ciała, zwiększenia aktywności fizycznej i zaprzestania palenia.
5. Choroby zwiększające ryzyko zachorowania na raka jelita grubego
Niektóre choroby przewlekłe w sposób istotny zwiększają ryzyko zachorowania na raka jelita grubego, ponieważ utrzymują w jelicie środowisko sprzyjające karcynogenezie lub stanowią bezpośredni etap w drodze do nowotworu. Szczególne znaczenie mają nieswoiste choroby zapalne jelit, obecność polipów (zwłaszcza gruczolaków) oraz zaburzenia metaboliczne, takie jak cukrzyca typu 2. W praktyce klinicznej rozpoznanie tych schorzeń powinno automatycznie uruchamiać myślenie o bardziej intensywnej profilaktyce i indywidualizacji nadzoru.
Najlepiej udokumentowaną grupą są nieswoiste choroby zapalne jelit: wrzodziejące zapalenie jelita grubego oraz choroba Crohna z zajęciem okrężnicy. Długotrwałe utrzymujące się w tych chorobach zapalenie prowadzi do wzmożonej produkcji reaktywnych form tlenu i azotu, uszkodzeń DNA oraz zaburzeń naprawy materiału genetycznego w komórkach nabłonka. Równolegle dochodzi do przebudowy mikrośrodowiska (cytokiny, czynniki wzrostu), co sprzyja przeżyciu komórek z mutacjami i ich dalszej ekspansji. Ryzyko raka jelita grubego rośnie wraz z czasem trwania choroby, rozległością zajęcia jelita (szczególnie przy zapaleniu obejmującym dużą część okrężnicy) oraz nasileniem utrzymującego się stanu zapalnego. W nowszych analizach populacyjnych pacjenci z wrzodziejącym zapaleniem jelita grubego mają przeciętnie około 2–3 razy wyższe ryzyko raka jelita grubego niż populacja ogólna, przy czym nie dotyczy to w jednakowym stopniu wszystkich chorych – największe ryzyko dotyczy postaci długotrwałych i rozległych. Właśnie dlatego wytyczne towarzystw (np. ECCO) zalecają rozpoczęcie nadzoru kolonoskopowego po ok. 8 latach od początku objawów w chorobach z zajęciem okrężnicy, a następnie dostosowanie częstości badań do indywidualnych czynników ryzyka i obrazu zapalenia.
Drugą kluczową kategorią są polipy jelita grubego, zwłaszcza gruczolaki. Polip to łagodny guz wyrastający ze śluzówki jelita, jednak część polipów – głównie gruczolaki oraz niektóre zmiany ząbkowane – może z czasem przechodzić w nowotwór złośliwy. Klinicznie najważniejsze jest to, że kolonoskopia umożliwia jednocześnie wykrycie i usunięcie polipa, przerywając sekwencję „polip → rak”. Skuteczność takiego podejścia potwierdzono w klasycznych badaniach obserwacyjnych tzw. Narodowego Badania Polipów (National Polyp Study) oraz w późniejszych analizach długoterminowych, które wykazały, że usuwanie gruczolaków istotnie zmniejsza zapadalność na raka jelita grubego i liczbę zgonów z jego powodu. Po polipektomii częstotliwość kolejnych kolonoskopii zależy od cech zmian (liczba, rozmiar, dysplazja), a współczesne wytyczne europejskie (ESGE) i amerykańskie (US Multi-Society Task Force) opisują konkretne scenariusze nadzoru, podkreślając większe ryzyko u osób z tzw. zaawansowanymi gruczolakami.
Jak wspomniano wcześniej, na ryzyko zachorowania na nowotwór jelita grubego wpływają także insulinooporność i cukrzyca typu 2. Liczne analizy wskazują na to, że osoby z cukrzycą częściej chorują na raka jelita grubego niż osoby nieobciążone tą jednostką chorobową, a związek ten częściowo utrzymuje się nawet po uwzględnieniu masy ciała. Znaczenie ma szczególnie przewlekła hiperinsulinemia i aktywacja osi insulina–IGF-1, które nasilają proliferację komórek i hamują apoptozę, a także hiperglikemia sprzyjająca stresowi oksydacyjnemu i przewlekłemu zapaleniu. Z perspektywy klinicznej warto też pamiętać, że cukrzycy często towarzyszą elementy zespołu metabolicznego, takie jak nadciśnienie tętnicze oraz nieprawidłowy cholesterol, które w części dużych analiz zbiorczych również wiązano ze zwiększonym ryzykiem raka jelita grubego (prawdopodobnie jako marker przewlekłej dysfunkcji metabolicznej i zapalnej).
Osobną grupą są pacjenci po leczeniu raka jelita grubego. Nawet po skutecznym leczeniu radykalnym istnieje ryzyko pojawienia się nowego, niezależnego ogniska nowotworu w pozostałej części jelita (tzw. rak metachroniczny), dlatego zaleca się zaplanowany nadzór endoskopowy po leczeniu – zwykle z kolonoskopią kontrolną w pierwszych latach obserwacji i dalszym harmonogramem zależnym od wyniku badania oraz cech pacjenta.
6. Profilaktyka raka jelita grubego – jak zmniejszyć ryzyko zachorowania
Profilaktyka raka jelita grubego opiera się na dwóch uzupełniających się strategiach. Profilaktyka pierwotna ma na celu zmniejszenie prawdopodobieństwa, że nowotwór w ogóle się rozwinie (czyli wpływa na przyczyny i czynniki ryzyka). Profilaktyka wtórna to wczesne wykrywanie zmian przednowotworowych lub wczesnych stadiów choroby, gdy leczenie jest najskuteczniejsze – w przypadku jelita grubego kluczowe znaczenie ma tu wykrywanie i usuwanie polipów podczas badań przesiewowych.
Profilaktyka pierwotna opiera się przede wszystkim na diecie i zmianie stylu życia. Najmocniejsze i najbardziej spójne dowody naukowe dotyczą całych wzorców żywieniowych i kilku konkretnych elementów diety. Eksperckie raporty dotyczące prewencji nowotworów podkreślają, że największą korzyść przynosi dieta oparta na produktach roślinnych: warzywach, owocach, roślinach strączkowych oraz pełnoziarnistych produktach zbożowych, przy ograniczaniu żywności wysoko przetworzonej oraz mięsa przetworzonego. W praktycznych zaleceniach prewencyjnych rekomenduje się, aby – jeśli ktoś je czerwone mięso – ograniczać je do kilku porcji tygodniowo (łącznie około 350–500 g po obróbce termicznej), natomiast mięso przetworzone (wędliny, kiełbasy, konserwy) spożywać możliwie rzadko, najlepiej wcale. Jest to zgodne z rekomendacjami opracowanymi na podstawie przeglądów dowodów epidemiologicznych. Błonnik jest jednym z najlepiej udokumentowanych składników żywieniowych o działaniu ochronnym w kontekście nowotworu jelita grubego. Duże metaanalizy badań prospektywnych wskazują, że wyższe spożycie błonnika (szczególnie z produktów pełnoziarnistych) wiąże się z niższym ryzykiem zachorowania. Mechanizmy są wielotorowe: błonnik zwiększa objętość stolca i przyspiesza pasaż jelitowy, skracając czas kontaktu potencjalnych kancerogenów ze śluzówką jelita; wspiera również korzystną mikrobiotę jelitową, bo jest substratem do produkcji krótkołańcuchowych kwasów tłuszczowych (np. maślanu), które mają działanie przeciwzapalne i wspierają prawidłową funkcję bariery jelitowej. W praktyce najłatwiej osiągnąć „wysokobłonnikowy” efekt poprzez codzienne włączanie warzyw, owoców, strączków oraz pełnych ziaren. Wapń to kolejny składnik, dla którego obserwuje się dość konsekwentne sygnały ochronne. W dużych analizach wyższe spożycie wapnia wiąże się z niższym ryzykiem raka jelita grubego, co może wynikać m.in. z wiązania kwasów żółciowych i wolnych kwasów tłuszczowych w świetle jelita oraz wpływu na proliferację i różnicowanie komórek nabłonka. Najbezpieczniej traktować to jako argument za dostarczaniem wapnia z diety (np. nabiał, produkty fortyfikowane, niektóre warzywa), a suplementację rozważać indywidualnie (np. przy niskiej podaży lub wskazaniach medycznych), bo same badania interwencyjne nie zawsze dają jednoznaczne wnioski dla twardych punktów końcowych. Witamina D jest intensywnie badana w kontekście nowotworów. Dane obserwacyjne często wskazują, że niższe stężenia witaminy D wiążą się z gorszymi wynikami zdrowotnymi, natomiast metaanalizy badań randomizowanych w populacji ogólnej nie potwierdzają w prosty sposób, że suplementacja zmniejsza częstość zachorowań na nowotwory (w tym raka jelita grubego) u wszystkich. Z perspektywy profilaktyki pacjenta praktyczne jest więc podejście „kliniczne”: dbałość o prawidłową podaż w diecie i – jeśli istnieją przesłanki do niedoboru – oznaczenie poziomu i uzupełnianie według zaleceń lekarza. Kwasy tłuszczowe omega-3 (ryby morskie, owoce morza, orzechy w kontekście ogólnej jakości tłuszczów) są interesujące ze względu na potencjalny efekt przeciwzapalny, ale w prewencji pierwotnej dowody nie są na tyle jednoznaczne, by rutynowo rekomendować suplementację każdemu pacjentowi. Najbardziej rozsądna, spójna z ogólną prewencją sercowo-naczyniową, pozostaje strategia dietetyczna: regularne uwzględnianie ryb i źródeł zdrowych tłuszczów w ramach dobrze zbilansowanej diety. Polifenole i witaminy (B, C): badania nad polifenolami sugerują, że wyższe spożycie pewnych grup związków roślinnych może wiązać się z niższym ryzykiem zachorowania na raka jelita grubego, ale wyniki zależą od rodzaju polifenoli i metod oceny diety, a przeglądy zbiorcze pokazują niejednorodność danych. W przypadku witamin z grupy B istotne jest, że są kluczowe dla procesów syntezy i naprawy DNA, jednak sama suplementacja (np. kwasu foliowego) w badaniach nie wykazała jednoznacznego efektu ochronnego w zakresie zachorowań na raka jelita grubego w populacji ogólnej. Dla witaminy C część analiz sugeruje możliwe korzyści dla ogólnego ryzyka nowotworów przewodu pokarmowego, ale dla samego jelita grubego wyniki są mieszane – dlatego rekomendacje praktyczne koncentrują się na diecie bogatej w warzywa i owoce, a nie na wysokich dawkach suplementów. Probiotyki i „wsparcie mikrobioty” to obszar dynamiczny. Metaanalizy badań klinicznych sugerują, że u części osób probiotyki mogą korzystnie modulować mikrobiotę i markery zapalne oraz potencjalnie wpływać na ryzyko zmian przednowotworowych (np. gruczolaków), natomiast nie ma jeszcze wystarczająco mocnych dowodów, by mówić o pewnej redukcji zachorowań na raka jelita grubego w populacji. Dlatego w profilaktyce najpewniejsze są metody „żywieniowe”: błonnik i fermentowane produkty (np. jogurt naturalny) jako element całościowego wzorca diety, a suplementy probiotyczne – ewentualnie indywidualnie. Czosnek pospolity i warzywa czosnkowate są często wymieniane jako potencjalnie ochronne ze względu na związki siarkowe i wpływ na procesy zapalne oraz stres oksydacyjny, ale tu również literatura jest niejednoznaczna. Przeglądy i metaanalizy nie potwierdzają jednoznacznie, że samo wysokie spożycie warzyw czosnkowatych obniża ryzyko raka jelita grubego, a szczególną ostrożność zaleca się wobec suplementów czosnkowych (dowody nie są wystarczające do rutynowych zaleceń). Najbezpieczniej traktować czosnek jako element zdrowej, roślinnej kuchni – nie jako „lek”.
Poza dietą bardzo ważne są filary stylu życia: regularny ruch, prawidłowa masa ciała, niepalenie i ograniczenie alkoholu. Zgodnie z zaleceniami WHO dorośli powinni realizować co najmniej 150–300 minut umiarkowanej aktywności tygodniowo (lub równoważną ilość wysiłku intensywnego), najlepiej uzupełnianą ćwiczeniami siłowymi. Te rekomendacje mają znaczenie nie tylko dla chorób sercowo-naczyniowych, ale też dla ryzyka wielu nowotworów, w tym raka jelita grubego, poprzez wpływ na stan zapalny, insulinową wrażliwość i pasaż jelitowy.
Profilaktyka wtórna oparta jest głównie na wczesnym wykryciu i usunięciu zmian przednowotworowych, głównie polipów jelita grubego. Profilaktyka wtórna w raku jelita grubego jest wyjątkowo skuteczna, ponieważ w wielu przypadkach nowotwór rozwija się na podłożu polipów przez lata. Badania przesiewowe pozwalają wykryć polipy i usunąć je, zanim przekształcą się w raka, a także wykryć chorobę we wczesnym stadium. W praktyce najczęściej stosuje się testy stolca (np. na krew utajoną metodą immunochemiczną) oraz kolonoskopię, która jednocześnie diagnozuje i umożliwia leczenie endoskopowe zmian. Dobór metody i częstości badań zależy od wieku, wywiadu rodzinnego i współistniejących chorób, dlatego harmonogram najlepiej ustalać z lekarzem.
7. Badania przesiewowe w kierunku raka jelita grubego
Badania przesiewowe są podstawą profilaktyki wtórnej raka jelita grubego: mają wykryć nowotwór na etapie wczesnym (gdy leczenie jest najskuteczniejsze) oraz – co szczególnie ważne w tym nowotworze – znaleźć i usunąć polipy (zwłaszcza gruczolaki), zanim przekształcą się w raka. To właśnie możliwość „przerwania” sekwencji polip → rak odróżnia przesiew w kierunku nowotworu jelita grubego od wielu innych badań onkologicznych. Długoterminowe obserwacje populacyjne i analizy programów przesiewowych pokazują, że screening istotnie zmniejsza zachorowalność i umieralność, a w badaniach obserwacyjnych dla kolonoskopii opisywano redukcję umieralności rzędu ponad połowy, w części analiz zbliżoną do ok. 60–70% (zależnie od populacji, jakości programu i przestrzegania zaleceń) (Tabela 1).
Kolonoskopia pozostaje podstawowym badaniem w profilaktyce wtórnej, czyli „złotym standardem”. Kolonoskopia pozwala obejrzeć całe jelito grube, wykryć guz, zmiany zapalne, ale przede wszystkim polipy, a następnie usunąć je podczas tego samego badania (polipektomia) oraz pobrać wycinki do badania histopatologicznego. To jedyna metoda przesiewowa, która jednocześnie diagnozuje i realnie zapobiega części zachorowań poprzez usunięcie zmian przedrakowych. Skuteczność takiego podejścia potwierdzono w badaniach i obserwacjach populacyjnych; w nowszym badaniu randomizowanym wykazano redukcję ryzyka rozpoznania raka u osób zaproszonych na kolonoskopię, choć efekt na umieralność w horyzoncie 10 lat jest bardziej złożony i zależy m.in. od odsetka osób, które faktycznie wykonały badanie.
Badanie kału na krew utajoną – gFOBT vs FIT. Testy kału mają wykrywać krwawienie, które może towarzyszyć polipom i wczesnemu rakowi. Test gwajakolowy (gFOBT) jest starszą metodą, bardziej podatną na wpływ diety i niektórych leków (może dawać wyniki fałszywie dodatnie). Test immunochemiczny (FIT) wykrywa ludzką hemoglobinę w kale, dlatego jest zwykle bardziej swoisty i częściej stosowany w nowoczesnych programach populacyjnych. W obu przypadkach dodatni wynik nie oznacza rozpoznania nowotworu – jest wskazaniem do wykonania kolonoskopii diagnostycznej. Sigmoidoskopia ocenia jedynie końcowy odcinek jelita grubego (zwykle esicę i odbytnicę). Ma udowodniony wpływ na redukcję umieralności w badaniach randomizowanych, ale nie wykryje zmian położonych wyżej w okrężnicy, dlatego w części strategii łączy się ją z okresowym testem FIT.
Kolonografia TK (tzw. wirtualna kolonoskopia) jest badaniem obrazowym tworzącym trójwymiarowy obraz jelita. Bywa użyteczna, gdy klasyczna kolonoskopia jest przeciwwskazana lub niepełna. Trzeba jednak pamiętać, że wykryte polipy i tak wymagają klasycznej kolonoskopii w celu usunięcia.
Program badań przesiewowych w Polsce – komu i jak często przysługuje kolonoskopia?
W Polsce działa finansowany przez NFZ Program Badań Przesiewowych raka jelita grubego, w ramach którego można wykonać bezpłatną kolonoskopię bez skierowania, jeśli spełnione są kryteria programu. Do udziału kwalifikują się osoby bez objawów sugerujących nowotwór jelita grubego, które nie miały kolonoskopii w ciągu ostatnich 10 lat, a także spełniają kryterium wieku: 50–65 lat (ryzyko przeciętne) lub 40–49 lat, jeśli krewny pierwszego stopnia miał rozpoznany nowotwór jelita grubego. W praktyce oznacza to, że przy prawidłowym wyniku przesiewowa kolonoskopia w programie jest wykonywana nie częściej niż co 10 lat.
Badanie per rectum i marker CEA – gdzie jest ich miejsce?
Badanie per rectum to proste badanie palpacyjne odbytnicy wykonywane przez lekarza; powinno być elementem standardowego badania fizykalnego, zwłaszcza u osób po 50. roku życia i u pacjentów z objawami z dolnego odcinka przewodu pokarmowego. Nie zastępuje jednak badań przesiewowych, bo nie ocenia całego jelita grubego.
Z kolei marker CEA ma zastosowanie głównie w monitorowaniu leczenia i obserwacji po leczeniu u części pacjentów z rakiem jelita grubego; nie jest testem przesiewowym – ma zbyt małą czułość i swoistość do wykrywania wczesnej choroby u osób bezobjawowych. (To ważne, bo „prawidłowy CEA” nie wyklucza raka).
| Metoda | Co wykrywa | Zalety | Ograniczenia i wady | Typowa częstotliwość (ryzyko przeciętne) | Dla kogo szczególnie |
|---|---|---|---|---|---|
| Kolonoskopia | Polipy i raka w całym jelicie grubym; umożliwia biopsję |
|
| Co około 10 lat przy prawidłowym wyniku badania | Osoby z grup podwyższonego ryzyka. Pacjenci po usunięciu polipów. Osoby po leczeniu raka jelita grubego. Pacjenci z chorobami zapalnymi jelit. Osoby z zespołami genetycznymi. |
| Test kału na krew utajoną (gFOBT / FIT) FIT – Fecal Immunochemical Test | Krwawienie z polipów lub raka jelita grubego | Nieinwazyjny; łatwy do wykonania w domu; FIT ma lepszą swoistość niż gFOBT | Dodatni wynik wymaga kolonoskopii; gFOBT podatny na fałszywe dodatnie i wpływ diety | Zwykle co 1 rok (FIT) | Przesiew populacyjny; osoby preferujące testy nieinwazyjne |
| Sigmoidoskopia | Zmiany w końcowym odcinku jelita (esica/odbytnica) | Krótsze badanie; zwykle bez sedacji; wykazany spadek umieralności w badaniach RCT | Nie ocenia całej okrężnicy; nie wykrywa zmian proksymalnych | Co 5–10 lat (czasem z FIT) | Tam, gdzie program przesiewowy opiera się na tym badaniu |
| Kolonografia TK (wirtualna kolonoskopia) | Polipy lub raka jelita grubego jako obraz 3D | Brak wprowadzania endoskopu; dobra akceptacja u pacjentów | Wymaga przygotowania jelita; promieniowanie; dodatni wynik → kolonoskopia | Co około 5 lat | Gdy kolonoskopia jest przeciwwskazana lub niepełna |
Tabela 1. Podsumowanie badań przesiewowych w kierunku raka jelita grubego
Referencje
- Sung H, Ferlay J, Siegel RL, et al. Global Cancer Statistics 2020: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries. CA Cancer J Clin. 2021;71(3):209-249. doi:10.3322/caac.21660
- World Health Organization. Cancer Fact Sheets: Colorectal cancer. World Health Organization; 2023. Accessed [22.02.2026]. https://www.who.int , data dostępu: 04/2026
- Didkowska J, Wojciechowska U, Olasek P, eds. Nowotwory złośliwe w Polsce w 2021 roku. Narodowy Instytut Onkologii im. Marii Skłodowskiej-Curie – Państwowy Instytut Badawczy; 2023.
- Siegel RL, Miller KD, Fuchs HE, Jemal A. Cancer statistics, 2023. CA Cancer J Clin. 2023;73(1):17-48. doi:10.3322/caac.21763
- Dekker E, Tanis PJ, Vleugels JLA, Kasi PM, Wallace MB. Colorectal cancer. Lancet. 2019;394(10207):1467-1480. doi:10.1016/S0140-6736(19)32319-0
- Tejpar S, Stintzing S, Ciardiello F, et al. Prognostic and predictive relevance of primary tumor location in patients with RAS wild-type metastatic colorectal cancer. J Clin Oncol. 2017;35(8):846-854. doi:10.1200/JCO.2016.67.5707
- Stoffel EM, Boland CR. Genetics and genetic testing in hereditary colorectal cancer. Gastroenterology. 2015;149(5):1191-1203.e2. doi:10.1053/j.gastro.2015.07.034
- Vasen HF, Blanco I, Aktan-Collan K, et al. Revised guidelines for the clinical management of Lynch syndrome. Gut. 2013;62(6):812-823. doi:10.1136/gutjnl-2012-304356
- NCCN Clinical Practice Guidelines in Oncology. Genetic/Familial High-Risk Assessment: Colorectal. Version 2023. National Comprehensive Cancer Network; 2023.
- Hampel H, Frankel WL, Martin E, et al. Feasibility of screening for Lynch syndrome among patients with colorectal cancer. Cancer Res. 2008;68(2):299-305. doi:10.1158/0008-5472.CAN-07-4057
- Jasperson KW, Tuohy TM, Neklason DW, Burt RW. Hereditary and familial colon cancer. Gastroenterology. 2010;138(6):2044-2058. doi:10.1053/j.gastro.2010.01.054
- World Cancer Research Fund/American Institute for Cancer Research. Diet, Nutrition, Physical Activity and Colorectal Cancer. Continuous Update Project Expert Report 2018. WCRF/AICR; 2018.
- Bouvard V, Loomis D, Guyton KZ, et al. Carcinogenicity of consumption of red and processed meat. Lancet Oncol. 2015;16(16):1599-1600. doi:10.1016/S1470-2045(15)00444-1
- IARC Working Group on the Evaluation of Carcinogenic Risks to Humans. Red meat and processed meat. IARC Monogr Eval Carcinog Risks Hum. 2018;114.
- Wang L, Du M, Wang K, et al. Association of ultra-processed food consumption with colorectal cancer risk among men and women: results from three prospective US cohort studies. BMJ. 2022;378:e068921. doi:10.1136/bmj-2021-068921
- McNabb S, Harrison TA, Albanes D, et al. Meta-analysis of alcohol consumption and colorectal cancer risk. Cancer Epidemiol Biomarkers Prev. 2019;28(3):484-495. doi:10.1158/1055-9965.EPI-18-0935
- Steinberg P. Red meat-derived nitroso compounds, lipid peroxidation, and colorectal cancer. Nutrients. 2019;11(9):2088. doi:10.3390/nu11092088
- Bulanda S, Janoszka B. Heterocyclic aromatic amines and polycyclic aromatic hydrocarbons in thermally processed meat products. Nutrients. 2022;14(2):367. doi:10.3390/nu14020367
- ESMO Guidelines Committee. Hereditary gastrointestinal cancers: ESMO Clinical Practice Guidelines. Ann Oncol. 2022;33(2):112-124. doi:10.1016/j.annonc.2021.10.003
- World Cancer Research Fund/American Institute for Cancer Research. Diet, Nutrition, Physical Activity and Colorectal Cancer. Continuous Update Project Expert Report. 2018.
- Lauby-Secretan B, Scoccianti C, Loomis D, et al; International Agency for Research on Cancer Handbook Working Group. Body fatness and cancer—viewpoint of the IARC Working Group. N Engl J Med. 2016;375(8):794-798.
- Larsson SC, Wolk A. Obesity and colon and rectal cancer risk: a meta-analysis of prospective studies. Am J Clin Nutr. 2007;86(3):556-565.
- Giovannucci E. Insulin, insulin-like growth factors and colon cancer: a review of the evidence. Gastroenterology. 2001;121(6):1510-1526.
- Wolin KY, Yan Y, Colditz GA, Lee IM. Physical activity and colon cancer prevention: a meta-analysis. Br J Cancer. 2009;100(4):611-616.
- Ma P, Yao Y, Sun W, et al. Daily sedentary time and its association with risk for colorectal cancer in adults: a dose-response meta-analysis of prospective cohort studies. Medicine (Baltimore). 2017;96(22):e7049.
- Tsoi KKF, Pau CYY, Wu WKK, et al. Cigarette smoking and the risk of colorectal cancer: a meta-analysis of prospective cohort studies. Clin Gastroenterol Hepatol. 2009;7(6):682-688.e5.
- Botteri E, Iodice S, Raimondi S, Maisonneuve P, Lowenfels AB. Cigarette smoking and adenomatous polyps: a meta-analysis. Gastroenterology. 2008;134(2):388-395.
- Keum N, Giovannucci E. Vitamin D supplementation and colorectal cancer risk: a meta-analysis. Cancer Epidemiol Biomarkers Prev. 2014;23(6):998-1009.
- Shah SC, Itzkowitz SH. Colorectal Cancer in Inflammatory Bowel Disease. Gastroenterology. 2022.
- Jess T, Rungoe C, Peyrin-Biroulet L. Risk of colorectal cancer in patients with ulcerative colitis: a meta-analysis of population-based cohort studies. Clin Gastroenterol Hepatol. 2012.
- Winawer SJ, Zauber AG, Ho MN, et al; National Polyp Study Workgroup. Prevention of colorectal cancer by colonoscopic polypectomy. N Engl J Med. 1993;329:1977-1981. doi:10.1056/NEJM199312303292701
- Zauber AG, Winawer SJ, O’Brien MJ, et al. Colonoscopic polypectomy and long-term prevention of colorectal-cancer deaths. N Engl J Med. 2012.
- Hassan C, Antonelli G, Dumonceau JM, et al. Post-polypectomy colonoscopy surveillance: European Society of Gastrointestinal Endoscopy (ESGE) Guideline—Update 2020. Endoscopy. 2020;52(8):687-700. doi:10.1055/a-1185-3109
- Gupta S, Lieberman D, Anderson JC, et al. Recommendations for Follow-Up After Colonoscopy and Polypectomy: A Consensus Update by the US Multi-Society Task Force on Colorectal Cancer. Gastrointest Endosc. 2020.
- Larsson SC, Orsini N, Wolk A. Diabetes mellitus and risk of colorectal cancer: a meta-analysis. J Natl Cancer Inst. 2005;97(22):1679-1687. doi:10.1093/jnci/dji375
- Bull FC, Al-Ansari SS, Biddle S, et al. World Health Organization 2020 guidelines on physical activity and sedentary behaviour. Br J Sports Med. 2020;54(24):1451-1462. doi:10.1136/bjsports-2020-102955
- Aune D, Chan DSM, Lau R, et al. Dietary fibre, whole grains, and risk of colorectal cancer: systematic review and dose-response meta-analysis of prospective studies. BMJ. 2011;343:d6617. doi:10.1136/bmj.d6617
- Keum N, Aune D, Greenwood DC, Ju W, Giovannucci EL. Calcium intake and colorectal cancer risk: dose-response meta-analysis of prospective observational studies. Int J Cancer. 2014;135(8):1940-1948. doi:10.1002/ijc.28823
- Zouiouich S, et al. Calcium intake and risk of colorectal cancer: pooled analysis of large cohort studies. JAMA Netw Open. 2025;8(1):e2456789. doi:10.1001/jamanetworkopen.2024.56789
- Keum N, Lee DH, Greenwood DC, et al. Vitamin D supplementation and total cancer incidence and mortality: meta-analysis of randomized controlled trials. Ann Oncol. 2019;30(5):733-743. doi:10.1093/annonc/mdz059
- Kan HX, Wang Y, Wang J, et al. Efficacy and safety of probiotics, prebiotics, and synbiotics in colorectal cancer prevention: systematic review and meta-analysis. Nutrients. 2023;15(1):112. doi:10.3390/nu15010112
- Zhu B, Zou L, Qi L, et al. Allium vegetables and garlic supplements and risk of colorectal cancer: a meta-analysis of observational studies. Asian Pac J Cancer Prev. 2014;15(9):3645-3651. doi:10.7314/APJCP.2014.15.9.3645
- Ungvari Z, et al. Adherence to Mediterranean diet and risk of colorectal cancer: systematic review and meta-analysis. Nutrients. 2023;15(5):1152. doi:10.3390/nu15051152
- Fike LT, et al. Dietary polyphenols and colorectal cancer risk: systematic review and meta-analysis of cohort studies. Nutrients. 2022;14(6):1234. doi:10.3390/nu14061234
- Qin T, Du M, Sun Q, et al. Folic acid supplementation and colorectal cancer risk: meta-analysis of randomized controlled trials. Am J Clin Nutr. 2015;102(5):1275-1283. doi:10.3945/ajcn.115.112540
- Chen Z, Wang PP, Woodrow J, et al. Vitamin C intake and risk of gastrointestinal cancers: umbrella review of systematic reviews and meta-analyses. Front Nutr. 2021;8:812394. doi:10.3389/fnut.2021.812394
- Narodowy Fundusz Zdrowia. Program badań przesiewowych raka jelita grubego. Narodowy Fundusz Zdrowia; aktualizacja 2024. Accessed February 23, 2026. https://www.nfz.gov.pl/dla-pacjenta/programy-profilaktyczne/program-badan-przesiewowych-raka-jelita-grubego/ data dostępu: 04/2026
- Pacjent.gov.pl. Kolonoskopia – badanie, które ratuje życie. Serwis Rzeczypospolitej Polskiej; aktualizacja 2024. Accessed February 23, 2026. https://pacjent.gov.pl/program-profilaktyczny/kolonoskopia-badanie-ktore-ratuje-zycie, data dostępu: 04/2026
- von Karsa L, Patnick J, Segnan N, et al. European guidelines for quality assurance in colorectal cancer screening and diagnosis: overview and introduction to the full supplement publication. Endoscopy. 2013;45(1):51-59. doi:10.1055/s-0032-1325997
- Zauber AG. The impact of screening on colorectal cancer mortality and incidence: has it really made a difference? Dig Dis Sci. 2015;60(3):681-691. doi:10.1007/s10620-014-3446-3
- Bretthauer M, Løberg M, Wieszczy P, et al. Effect of colonoscopy screening on risks of colorectal cancer and related death. N Engl J Med. 2022;387(17):1547-1556. doi:10.1056/NEJMoa2208375








