Co warto wiedzieć o progresji choroby
Rak jelita grubego to jeden z najczęściej występujących nowotworów złośliwych w Polsce i na świecie. Współczynniki zachorowalności są niższe u kobiet niż u mężczyzn — według danych Krajowego Rejestru Nowotworów w 2022 roku w Polsce na raka jelita grubego zachorowało 10,3 tys. mężczyzn i 8,5 tys. kobiet, co czyni go trzecim, co do częstości występowania, nowotworem u mężczyzn (po raku prostaty i płuca) i drugim u kobiet (po raku piersi). W ostatnich 25 latach w większości rozwiniętych krajów świata zachorowalność rośnie, a umieralność maleje lub pozostaje bez zmian. Wyjątkiem są Stany Zjednoczone Ameryki Północnej, gdzie obserwuje się zmniejszenie zachorowalności i umieralności. Wczesne wykrycie ma kluczowe znaczenie dla skuteczności leczenia, ponieważ rak jelita grubego zazwyczaj rozwija się przez dłuższy czas bez wyraźnych objawów klinicznych.
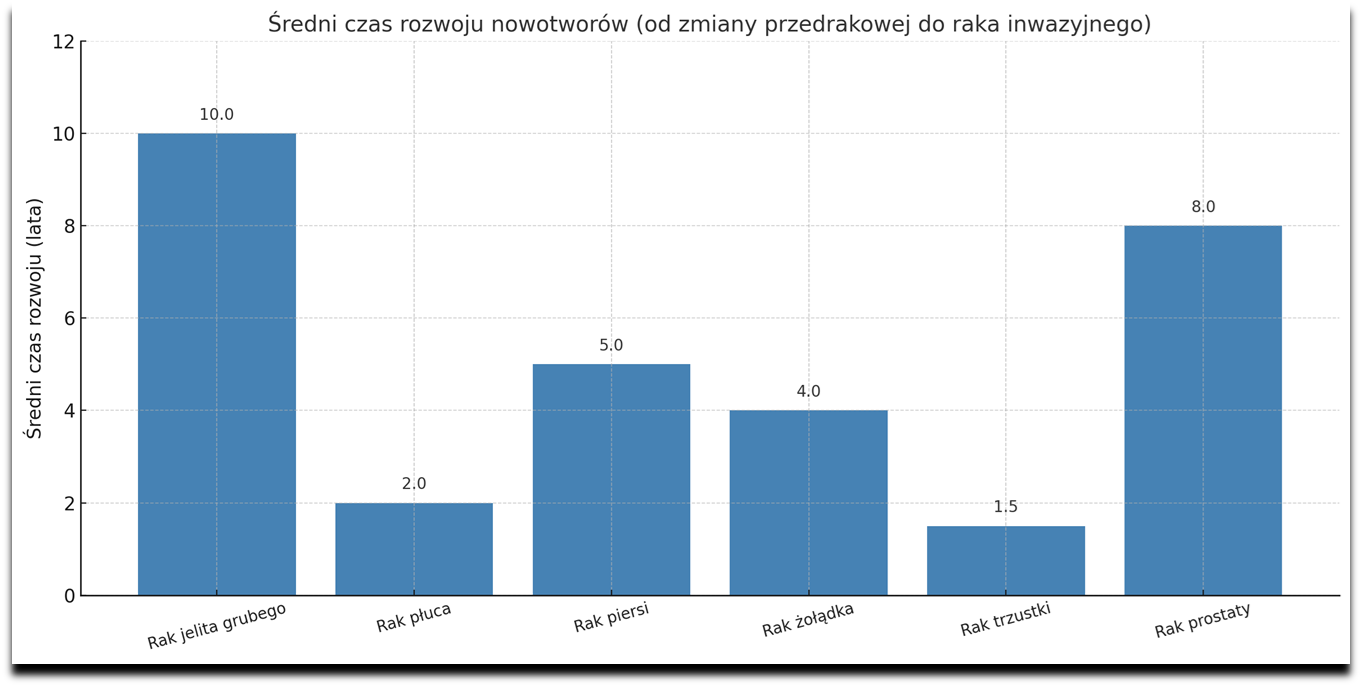
Wykres opracowany przez autorkę artykułu.
Od polipu do raka – jak przebiega proces rozwoju nowotworu jelita grubego?
Rak jelita grubego zazwyczaj rozwija się powoli –zmiana nowotworowa najczęściej powstaje z polipa gruczolakowatego. Tempo progresji może się różnić: niektóre guzy pozostają bezobjawowe i rosną wolno, inne mogą rozwinąć się agresywnie. W większości przypadków proces przekształcania łagodnych polipów w nowotwór złośliwy trwa od 7 do 15 lat. Ta stosunkowo powolna progresja daje możliwość wykrycia i usunięcia zmian przedrakowych podczas badań przesiewowych, takich jak kolonoskopia.
| Etap | Opis zmian | Charakter zmian |
|---|---|---|
| 1. Prawidłowy nabłonek | Brak zmian | Nabłonek bez nieprawidłowości |
| 2. Gruczolak – inicjacja | Pojawienie się małego gruczolaka (polipa) | Nadmierna proliferacja komórek |
| 3. Gruczolak – progresja | Wzrost polipa | Powiększenie i rozwój dysplazji |
| 4. Gruczolak o dużym stopniu dysplazji | Zaawansowany gruczolak z zaburzoną architekturą | Dalszy rozwój dysplazji |
| 5. Rak inwazyjny | Nowotwór złośliwy naciekający ścianę jelita | Możliwość przerzutów |
Tabela opracowana przez autorkę artykułu.
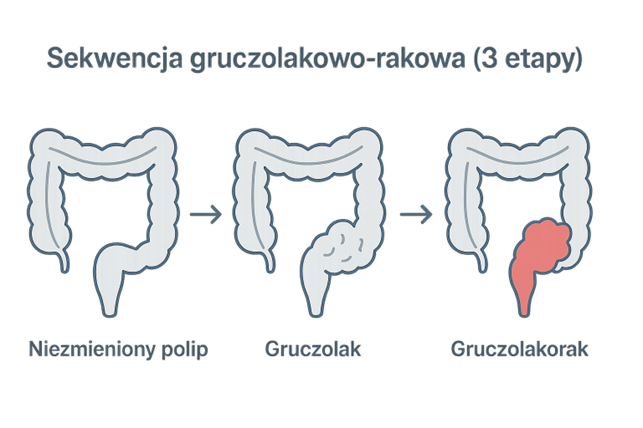 Grafika poglądowa została opracowana przez autorkę artykułu na podstawie wiedzy medycznej z wykorzystaniem narzędzi AI.
Grafika poglądowa została opracowana przez autorkę artykułu na podstawie wiedzy medycznej z wykorzystaniem narzędzi AI.
Na podstawie publikacji Hassan C, Antonelli G, Dumonceau J‑M, et al. Post-polypectomy colonoscopy surveillance: European Society of Gastrointestinal Endoscopy (ESGE) Guideline – Update 2020. Endoscopy. 2020;52(8):687–700. doi:10.1055/a-1185-3109.
Czynniki wpływające na tempo rozwoju raka jelita grubego
- Dieta – zbyt duża ilość spożywanych kalorii, przetworzona żywność, czerwone mięso, tłuszcze nasycone, alkohol, niska podaż błonnika, niedobór witamin (np. witaminy D, witaminy C) i składników mineralnych (np. wapnia, selenu, cynku) może osłabiać organizm i zwiększać ryzyko rozwoju nowotworu.
- Styl życia (siedzący tryb życia)
- Choroby współistniejące (wrzodziejące zapalenie jelita grubego, choroba Crohna, cukrzyca, otyłość)
- Wiek i płeć pacjenta (>50 rż, płeć męska)
- Czynniki genetyczne (zespół Lyncha – mutacje genów naprawy DNA dziedziczone autosomalnie dominująco, zwykle MLH1, MSH2, MSH3; ryzyko zachorowania 70-80%; rodzinna polipowatość gruczolakowa – dziedziczona autosomalnie dominująco mutacja genów APC, ryzyko zachorowania 100%; zespół Peutza-Jeghersa; zespół Cowden). Niektóre formy dziedziczne raka jelita grubego mogą rozwijać się szybciej niż formy sporadyczne. Mutacje genetyczne mogą wpływać na agresywność nowotworu i jego tempo wzrostu.
Mikroflora jelitowa odgrywa złożoną rolę w rozwoju nowotworów, zarówno promując, jak i hamując ten proces. Z jednej strony, niektóre bakterie jelitowe, mogą uwalniać toksyny uszkadzające DNA i sprzyjać rozwojowi raka jelita grubego. Z drugiej strony, zdrowa mikroflora jelitowa, bogata w korzystne bakterie, może działać ochronnie, modulując odpowiedź immunologiczną i zmniejszając stan zapalny, który jest czynnikiem ryzyka wielu nowotworów.
Oto dietetyczne zalecenia wspierające zdrową mikrobiotę jelitową, które mogą również przyczyniać się do zmniejszenia ryzyka raka jelita grubego:
- Jedz dużo błonnika pokarmowego
- Błonnik jest „pokarmem” dla bakterii jelitowych (działa jak prebiotyk).
- Fermentując błonnik, bakterie produkują maślan, który działa przeciwnowotworowo.
- Źródła:
- Warzywa (kapusta, brokuły, marchew, cebula)
- Owoce (jabłka, gruszki, jagody)
- Rośliny strączkowe (soczewica, fasola, ciecierzyca)
- Produkty pełnoziarniste (płatki owsiane, chleb razowy)
- Włącz do diety produkty fermentowane
- Zawierają naturalne probiotyki – korzystne bakterie.
- Wzmacniają różnorodność mikrobioty i działają przeciwzapalnie.
- Źródła:
- Jogurt naturalny, kefir, maślanka
- Kiszone ogórki, kapusta kiszona, kimchi
- Zakwas z buraków, kombucha
- Spożywaj prebiotyki
- To składniki żywności, które pobudzają wzrost dobrych bakterii.
- Źródła:
- Czosnek, cebula, por
- Banany (szczególnie lekko niedojrzałe)
- Cykoria, topinambur
- Szparagi, seler naciowy
- Pij odpowiednią ilość wody
- Wspomaga trawienie i fermentację błonnika.
- Ułatwia wydalanie toksyn z organizmu.
- Ogranicz spożycie:
- Czerwonego i przetworzonego mięsa (wędliny, parówki, kiełbasy)
- Tłuszczów trans i nasyconych (fast food, margaryny utwardzane)
- Cukru i słodyczy – sprzyjają rozwojowi szkodliwych bakterii
- Alkoholu i sztucznych słodzików – mogą zaburzać równowagę mikroflory
- Wspieraj mikroflorę stylem życia
- Ruch i aktywność fizyczna – poprawiają perystaltykę i wpływają korzystnie na mikrobiotę.
- Sen i redukcja stresu – stres może wpływać negatywnie na skład mikroflory.
Około 25% zachorowań na raka jelita grubego ma tło dziedziczne, a za pozostałe przypadki odpowiadają modyfikowalne czynniki środowiskowe.
Stadia rozwoju raka jelita grubego i ich charakterystyka
Klasyfikacja TNM to system oceny stopnia zaawansowania nowotworów złośliwych. Skrót TNM pochodzi od angielskich słów: tumor (guz), node (węzeł chłonny) i metastasis (przerzut). System ten pozwala na dokładne opisanie wielkości guza pierwotnego, obecności lub braku przerzutów do węzłów chłonnych oraz obecności lub braku przerzutów odległych, co ma kluczowe znaczenie dla planowania leczenia i określania rokowania.
| TNM | Stopień | Opis |
|---|---|---|
| T – guz pierwotny | Tis | Rak in situ – nowotwór ograniczony do błony śluzowej |
| T1 | Guz nacieka błonę podśluzową | |
| T2 | Guz nacieka warstwę mięśniową jelita | |
| T3 | Guz nacieka przez ścianę mięśniową do tkanki okołojelitowej | |
| T4a | Guz nacieka otrzewną trzewną | |
| T4b | Guz nacieka sąsiednie narządy lub struktury | |
| N – węzły chłonne | N0 | Brak przerzutów do regionalnych węzłów chłonnych |
| N1a | Przerzuty w 1 regionalnym węźle chłonnym | |
| N1b | Przerzuty w 2–3 węzłach chłonnych | |
| N1c | Guzki nowotworowe w tkance tłuszczowej okołojelitowej bez obecności w węzłach | |
| N2a | Przerzuty w 4–6 regionalnych węzłach chłonnych | |
| N2b | Przerzuty w ≥7 regionalnych węzłach chłonnych | |
| M – przerzuty odległe | M0 | Brak przerzutów odległych |
| M1a | Przerzuty w jednym narządzie (np. wątroba, płuca) | |
| M1b | Przerzuty w więcej niż jednym narządzie lub w otrzewnej | |
| M1c | Przerzuty w otrzewnej i co najmniej jednym innym narządzie |
Brierley JD, Van Eycken E, Rous BA, Giuliani M, O’Sullivan B, eds. TNM Classification of Malignant Tumours. 9th ed. Hoboken, NJ: John Wiley & Sons; 2025. ISBN 978-1-394-21685-7
Uproszczony podział na stadia (stopnie zaawansowania) raka jelita grubego
| Stadium 0 | rak przedinwazyjny (carcinoma in situ) |
| Stadium I | rak ograniczony do błony śluzowej |
| Stadium II | rak naciekający głębsze warstwy ściany jelita |
| Stadium III | rak z przerzutami do węzłów chłonnych |
| Stadium IV | rak z przerzutami odległymi |
Na podstawie: Brierley JD, Van Eycken E, Rous BA, Giuliani M, O’Sullivan B, eds. TNM Classification of Malignant Tumours. 9th ed. Hoboken, NJ: John Wiley & Sons; 2025. ISBN 978-1-394-21685-7.
Ogólny wskaźnik 5-letniego przeżycia w przypadku raka jelita grubego wynosi w Polsce około 44-45%. Jednakże, rokowania zależą w dużej mierze od stadium zaawansowania nowotworu w momencie diagnozy. Tempo progresji między kolejnymi stadiami jest zróżnicowane i zależy od wielu czynników, w tym od biologii guza nowotworowego.
Szczegółowe rokowania w zależności od stadium (5-letnie przeżycie)
| Stadium | Przeżycie 5-letnie |
| Stadium 0 | 90–100% |
| Stadium I | 90–100% |
| Stadium II | 50–80% |
| Stadium III | 30–60% |
| Stadium IV | 10–20% |
Na podstawie: Bouvier A‑M, et al. Differences in survival and recurrence of colorectal cancer by stage across population-based European registries. International Journal of Cancer. 2024.
Wczesne stadium = znacznie większe szanse na przeżycie.
Stadium 0 lub I daje niemal pełne przeżycie przez co najmniej 5 lat
Stadium II–III: rokowanie i skuteczność leczenia są zróżnicowane i zależą od wielu czynników, takich jak lokalizacja guza, wiek pacjenta czy zastosowana terapia. W porównaniu z wcześniejszymi stadiami choroby, odsetek przeżyć istotnie się zmniejsza.
Stadium IV: tylko nieliczni pacjenci przeżywają 5 lat, często są to osoby bardzo dobrze reagujące na leczenie lub kwalifikujące się do leczenia operacyjnego przerzutów.
Średnia krajowa (ok. 44–45%) przekłamuje spore różnice między pacjentami z rozpoznaniem we wczesnym a zaawansowanym stadium.
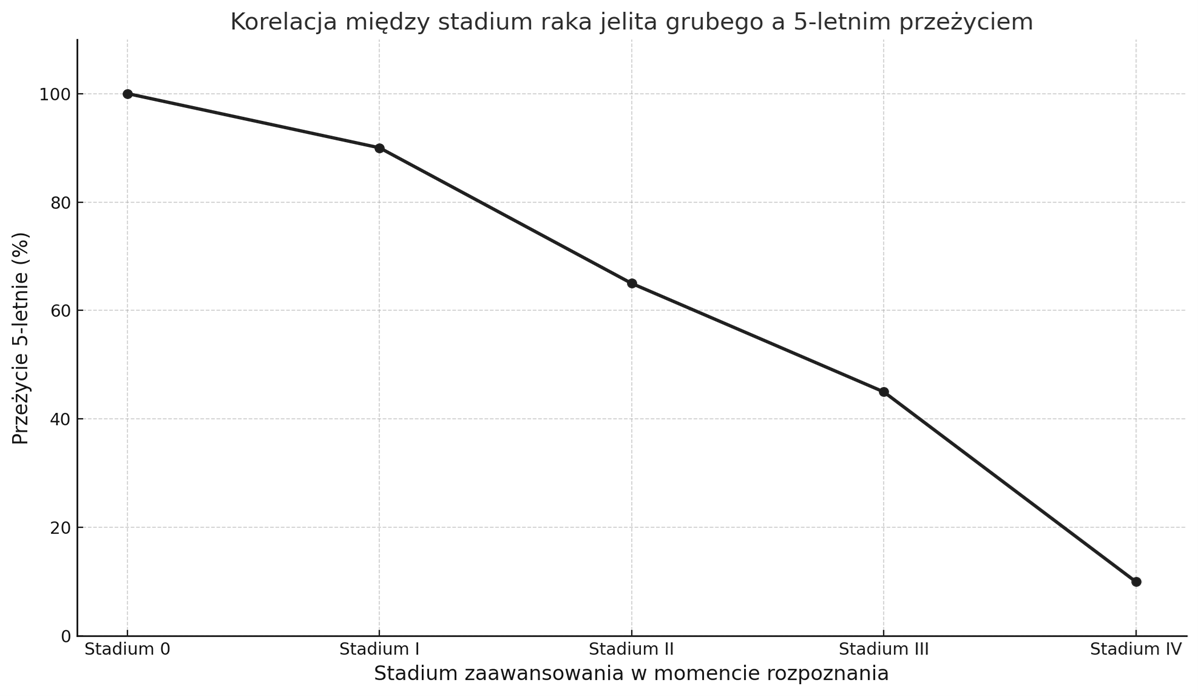
Wykres poglądowa została opracowany przez autorkę artykułu.
Przerzuty raka jelita grubego – kiedy i gdzie się pojawiają?
Przerzuty raka jelita grubego najczęściej lokalizują się w wątrobie, płucach, otrzewnej i węzłach chłonnych.
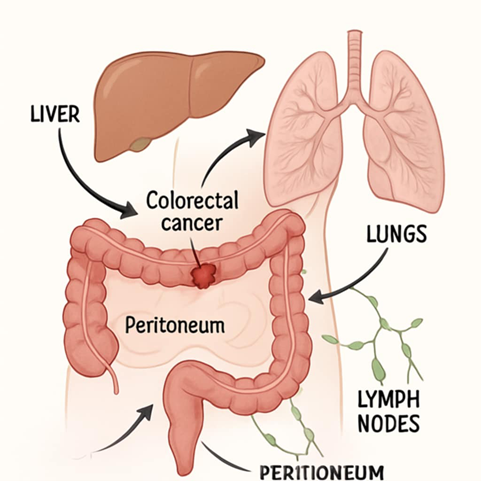
Opis do grafiki: Angielski (EN) – Polski (PL): Liver – Wątroba, Lungs – Płuca, Lymph nodes – Węzły chłonne, Peritoneum – Otrzewna Colorectal cancer – Rak jelita grubego
Grafika poglądowa została opracowana przez autorkę artykułu na podstawie wiedzy medycznej z wykorzystaniem narzędzi AI.
Średni czas progresji raka jelita grubego do kolejnego stadium jest trudny do ujęcia w jednoznacznych liczbach, ponieważ zależy od wielu czynników. Jednak na podstawie badań klinicznych, obserwacji naturalnego przebiegu choroby i danych epidemiologicznych można podać szacunkowe informacje dla poszczególnych etapów rozwoju:
| Stadium | Średni czas progresji do kolejnego stadium |
| 0/I | 5–10 lat |
| I/II | średnio 1–2 lata |
| II/III | średnio 6–18 miesięcy |
| III/IV | często < 1 rok |
Tabela Na podstawie: European Commission. European guidelines for quality assurance in colorectal cancer screening and diagnosis.
Etapy powstawania przerzutów:
- Transformacja nowotworowa i inwazja lokalna
- Komórki guza nabywają zdolność do migracji i niszczenia otaczających tkanek.
- Uwalniają enzymy (np. metaloproteinazy), które rozkładają macierz międzykomórkową.
- Przebijają się przez błonę podstawną i naciekają sąsiednie tkanki.
- Wniknięcie do naczyń krwionośnych lub chłonnych (intrawazacja)
- Komórki nowotworowe przenikają do naczyń (najczęściej naczyń włosowatych lub limfatycznych).
- W tym momencie stają się komórkami krążącymi (CTC – circulating tumor cells).
- Transport w krwiobiegu lub chłonce
- Komórki nowotworowe krążą w organizmie.
- Muszą przetrwać warunki stresowe (ciśnienie krwi, układ odpornościowy).
- Zatrzymanie i wynaczynienie (ekstrawazacja)
- Komórki zatrzymują się w kapilarach konkretnego narządu (np. wątroba, płuca, kości).
- Przenikają przez ścianę naczynia do otaczającej tkanki (np. miąższu wątroby).
- Kolonizacja – wzrost nowego guza
- Komórki nowotworowe tworzą mikroskopowe przerzuty (mikrometastazy).
- Jeśli środowisko lokalne jest sprzyjające, zaczynają się dzielić i tworzyć makroskopowy guz przerzutowy.
- Muszą też zapewnić sobie unaczynienie (angiogenezę) – czyli tworzenie nowych naczyń krwionośnych.
Wykrycie nowotworu przed wystąpieniem przerzutów znacząco poprawia rokowanie. W przypadku ograniczonej liczby przerzutów do wątroby warto rozważyć metastazektomię, która pozwala na uzyskanie u 40% chorych przeżyć 5-letnich i u około 20% – 10-letnich. Zastosowanie u chorych z rozsiewem ograniczonym do otrzewnej operacji cytoredukcyjnej poprzedzającej zastosowanie HIPEC może istotnie wydłużać całkowite przeżycie w porównaniu z wyłączną systemową chemioterapią. Mediana przeżycia chorych w dobrym stanie ogólnym leczonych systemowo przekracza 2 lata.
Objawy kliniczne a stadium rozwoju raka jelita grubego
Niestety, początkowe stadia raka jelita grubego często przebiegają bezobjawowo lub z objawami nieswoistymi, co utrudnia wczesną diagnozę.
Charakterystyczne objawy, na które należy zwrócić uwagę (zazwyczaj występują dopiero w późniejszych stadiach choroby):
- Zmiana rytmu wypróżnień (zaparcia, biegunka)
- Krew w kale (jawna lub utajona), uczucie niepełnego wypróżnienia
- Ból brzucha, wzdęcia
- Niedokrwistość z niedoboru żelaza
- Niedrożność jelit
- Utrata masy ciała
- Ogólne osłabienie
Późne pojawienie się objawów jest jednym z powodów, dlaczego badania przesiewowe są tak istotne w wykrywaniu raka jelita grubego we wczesnym stadium!
| Lokalizacja guza | Typowe objawy | Uwagi kliniczne |
| Prawa połowa okrężnicy (kątnica, wstępnica, zgięcie wątrobowe) | – Utajone krwawienie → przewlekła anemia – Osłabienie, zmęczenie – Niespecyficzne bóle brzucha – Uczucie pełności – Spadek masy ciała | Luźniejsza treść jelitowa – guz może rosnąć długo bez objawów niedrożności. Zmiany są późno zauważane. |
| Lewa połowa okrężnicy (zstępnica, esica, zgięcie śledzionowe) | – Zaparcia na przemian z biegunkami – Cienkie, „ołówkowate” stolce – Uczucie niepełnego wypróżnienia – Świeża krew w stolcu – Bóle kolkowe | Treść kałowa jest bardziej uformowana, guz szybciej prowadzi do częściowej lub całkowitej niedrożności. |
| Odbytnica (rak odbytnicy) | – Krwawienia z odbytu (jasnoczerwona krew) – Parcie na stolec („tenesmus”) – Ból przy defekacji – Uczucie obecności ciała obcego w odbycie | Objawy często mylone z hemoroidami. Guz może być wyczuwalny w badaniu per rectum. |
| Objaw | Prawa strona | Lewa strona | Odbytnica |
| Niedokrwistość (z niedoboru żelaza) | ✅ Częsta | Rzadsza | Rzadka |
| Krwawienie do przewodu pokarmowego | Utajone | Często widoczne | Bardzo częste, jasna krew |
| Zmiana rytmu wypróżnień | Rzadka | Częsta | Bardzo częsta |
| Ból brzucha | Tępy, niespecyficzny | Kolkowy | Ból przy defekacji |
| Niedrożność jelit | Rzadka (duża średnica) | Częstsza | Możliwa, ale późno |
Tabela na podstawie: Shinkins B, et al. Systematic review of clinical features of suspected colorectal cancer in primary care.
Metody diagnostyczne w ocenie stopnia zaawansowania i tempa progresji raka jelita grubego
W ocenie stopnia zaawansowania i tempa progresji raka jelita grubego stosuje się szereg metod diagnostycznych, które pozwalają na precyzyjne określenie stadium choroby oraz planowanie odpowiedniego leczenia.
- Badania endoskopowe (kolonoskopia, rektoskopia) – podstawowe badania, pozwalające na wzrokową ocenę jelita grubego, pobranie wycinków do badania histopatologicznego oraz usunięcie polipów, które mogą być stanami przedrakowymi. W Polsce program badań przesiewowych oferuje bezpłatną kolonoskopię osobom w wieku 50-65 lat, a także młodszym, jeśli w rodzinie wystąpił rak jelita grubego.
- Badania obrazowe (tomografia komputerowa, rezonans magnetyczny) – pozwalają na określenie stadium zaawansowania nowotworu i zaplanowanie odpowiedniego leczenia.
- Badania laboratoryjne (markery nowotworowe jak CEA i CA 19-9) – pomocne w trakcie monitorowania choroby w trakcie leczenia oraz przy wykrywaniu wczesnej wznowy. Nie mają zastosowania w diagnostyce u Pacjentów bez rozpoznanej choroby nowotworowej.
- Badanie histopatologiczne – analiza próbki tkanki nowotworowej pobranej podczas kolonoskopii lub innej procedury. To kluczowe badanie, które pozwala dokładnie określić typ, stopień zaawansowania i złośliwości raka.
- Badania molekularne – pozwalają na zidentyfikowanie konkretnych mutacji genetycznych, które występują w komórkach nowotworu. Dzięki temu możliwa jest personalizacja terapii, co zwiększa skuteczność leczenia.
Mutacje w genach RAS i BRAF: Wykrycie mutacji w tych genach jest istotne przy wyborze leczenia anty-EGFR u pacjentów z przerzutowym rakiem jelita grubego;
Stopień niestabilności mikrosatelitarnej/ czynności genów naprawy niesparowanych zasad DNA (MSI/MMR): Badanie zalecane niezależnie od stopnia zaawansowania (we wczesnych stopniach zaawansowania ma wartość prognostyczną, w chorobie przerzutowej jest czynnikiem predykcyjnym dla immunoterapii)
Znaczenie kolonoskopii w wykrywaniu wczesnych stadiów raka jelita grubego
Złotym standardem w wykrywaniu raka jelita grubego jest kolonoskopia. Badanie to pozwala na wykrycie zmian przedrakowych (polipów) oraz wczesnych stadiów raka, kiedy choroba rozwija się jeszcze miejscowo i ma najlepsze rokowanie.
Warto podkreślić, że kolonoskopia nie tylko umożliwia diagnostykę, ale także pozwala na wykonanie zabiegu terapeutycznego (usunięcie polipów), co może zapobiec rozwojowi raka. Usunięcie polipu podczas kolonoskopii może zatrzymać sekwencję gruczolakowato-rakową i tym samym zapobiec rozwojowi inwazyjnego nowotworu.
| Grupa ryzyka | Rekomendacja |
| Osoby po 50. r.ż. (standard) | Co 10 lat (jeśli wynik prawidłowy) |
| Osoby z polipami w wywiadzie | Co 3–5 lat |
| Osoby z rakiem jelita grubego w rodzinie | Od 40. r.ż. lub 10 lat przed wiekiem zachorowania krewnego |
| Osoby z nieswoistymi zapaleniami jelit | Częściej – wg zaleceń gastrologa |
Tabela na podstawie wiedzy własnej autora.
Nowoczesne metody leczenia a progresja raka jelita grubego
Nowoczesne metody leczenia raka jelita grubego są zróżnicowane i obejmują różne podejścia, które mają na celu nie tylko leczenie samej choroby, ale także poprawę jakości życia pacjentów oraz spowolnienie progresji nowotworu.
Oto kilka kluczowych metod:
- Chirurgia: Jest to jedna z najważniejszych metod leczenia raka jelita grubego, szczególnie w przypadkach, gdy nowotwór jest we wczesnym stadium. Obejmuje resekcję guza pierwotnego z regionalnymi węzłami chłonnymi oraz węzłami klinicznie podejrzanymi o przerzuty drogą laparotomii lub laparoskopii. W chorobie przerzutowej wykonuje się resekcję guza pierwotnego i metastazektomię (jeżeli przerzuty nie są resekcyjne, usunięcie guza pierwotnego wykonuje się ze wskazań klinicznych tj. niedrożność, istotne krwawienie).
- Chemioterapia: Używana jest do niszczenia komórek nowotworowych lub spowolnienia ich wzrostu. Stosuje się ją, aby zniszczyć komórki nowotworowe lub spowolnić ich wzrost. Chemioterapia uzupełniająca jest standardem w III stopniu zaawansowania. W II stopniu rozważa się ją u pacjentów, u których występują czynniki związane z gorszym rokowaniem. Zawiera Fluoropirymidynę (Fluorouracyl z Folinianem Wapniowym lub Kapecytabina) +/- Oksaliplatyna. Jest stosowana przez 6 miesięcy.
W przypadku zaawansowanej choroby nowotworowej stosowana jest chemioterapia paliatywna (czyli leczenie mające na celu spowolnienie choroby i złagodzenie objawów, a nie całkowite wyleczenie), która wpływa na przedłużenie życia pacjentów. Dobór schematu chemioterapii zależy od cech klinicznych pacjenta oraz cech molekularnych guza.
- Terapie celowane: Skupiają się na specyficznych molekułach i mechanizmach biologicznych, które są zaangażowane w rozwój raka (mutacja BRAF V600E, amplifikacja HER2). Udział w badaniach klinicznych może dać pacjentom dostęp do nowoczesnych terapii, które są w fazie testów, a także przyczynić się do postępu w badaniach nad rakiem jelita grubego.
- Immunoterapia: Wykorzystuje układ odpornościowy organizmu do zwalczania nowotworu. Leki takie jak inhibitory punktów kontrolnych (np. Pembrolizumab) mogą być skuteczne, zwłaszcza w przypadku raka jelita grubego ze stwierdzoną niestabilnością mikrosatelitarną.
- Radioterapia – ma największe znaczenie w raku odbytnicy, gdzie jest standardem leczenia w stadium II–III. Stosowana z chemioterapią przed operacją, znacząco poprawia wyniki leczenia i ogranicza ryzyko nawrotów. Dodatkowo, może zmniejszyć rozmiar guza i ułatwić jego usunięcie. Radioterapię pooperacyjną stosuje się rzadziej – głównie wtedy, gdy nie można było zastosować radioterapii przed operacją lub gdy w badaniu pooperacyjnym stwierdzono dodatnie marginesy (pozostawienie komórek nowotworowych na brzegu wyciętej tkanki). W zaawansowanych stadiach choroby, gdy rak jelita grubego powoduje ból lub inne objawy np. krwawienie z guza, radioterapia może być stosowana w celu łagodzenia tych dolegliwości, poprawiając jakość życia pacjenta.
- Terapie wspomagające: Skupiają się na objawowym łagodzeniu dolegliwości, związanych z chorobą nowotworową. Obejmują np. leki przeciwbólowe, leki przeciwwymiotne, leki na zaparcia/ biegunkę. Bardzo istotne jest również leczenie żywieniowe oraz terapie psychologiczne, które pomagają pacjentom radzić sobie z efektami ubocznymi leczenia i poprawiają ich jakość życia.
Obserwacja po radykalnym leczeniu
W I stopniu zaawansowania nie jest zalecane prowadzenie regularnych kontroli (z wyjątkiem kolonoskopii).
W II-III stopniu zaawansowania kontrola po leczeniu obejmuje:
- badania przedmiotowe i podmiotowe co 3-6 miesięcy przez 2 lata i co 6 miesięcy przez 3 lata
- oznaczanie stężenia CEA (antygen karcinoembrionalny – marker nowotworowy oznaczany z krwi, pomocny w monitorowaniu choroby) co 3-6 miesięcy przez 2 lata i co 6 miesięcy przez 3 lata
- TK (tomografia komputerowa) klatki piersiowej, jamy brzusznej i miednicy co 6-12 miesięcy przez 5 lat
W IV stopniu zaawansowania (po radykalnym leczeniu operacyjnym) TK (tomografia komputerowa) klatki piersiowej, jamy brzusznej i miednicy co 3-6 miesięcy przez 2 lata i co 6-12 miesięcy przez 3 lata; pozostałe badania jak w stopniach II-III.
Profilaktyka raka jelita grubego – jak zmniejszyć ryzyko i spowolnić rozwój choroby?
Profilaktyka raka jelita grubego jest kluczowa, ponieważ wiele przypadków można zapobiec przez wprowadzenie zdrowych nawyków oraz regularne badania przesiewowe. Oto kilka skutecznych strategii, które mogą pomóc w zmniejszeniu ryzyka oraz spowolnieniu rozwoju choroby:
- Zrównoważona dieta: Spożywanie diety bogatej w błonnik (owoce, warzywa, pełnoziarniste produkty) może pomóc w utrzymaniu zdrowego układu pokarmowego. Ograniczenie spożycia czerwonego i przetworzonego mięsa, a także tłuszczów nasyconych, może zmniejszyć ryzyko zachorowania.
- Aktywność fizyczna: Regularna aktywność fizyczna (minimum 150 minut umiarkowanej aktywności tygodniowo) może pomóc w utrzymaniu zdrowej masy ciała oraz zmniejszeniu ryzyka raka jelita grubego.
- Unikanie palenia i umiarkowane spożycie alkoholu: Palenie tytoniu i nadmierne spożycie alkoholu są związane z wyższym ryzykiem wielu nowotworów, w tym raka jelita grubego. Ograniczenie tych czynników ryzyka może pomóc w profilaktyce.
- Regularne badania przesiewowe: Osoby w grupie ryzyka (np. osoby powyżej 50. roku życia lub z rodzinną historią raka jelita grubego) powinny regularnie poddawać się badaniom przesiewowym, takim jak kolonoskopia. Wczesne wykrycie polipów lub zmian nowotworowych może znacznie zwiększyć szanse na skuteczne leczenie. Przydatne jest również badanie na obecność krwi utajonej w kale (co 1–2 lata). Pomaga wykryć niewidoczne krwawienia, które mogą świadczyć o polipach lub raku.
- Świadomość i edukacja: Zrozumienie czynników ryzyka oraz symptomów raka jelita grubego może pomóc w szybszym reagowaniu na niepokojące objawy. Edukacja na temat zdrowego stylu życia oraz dostępnych badań przesiewowych jest kluczowa. U niektórych pacjentów z wysokim ryzykiem (np. FAP – rodzinna polipowatość gruczolakowata – dziedziczna choroba, w której w jelicie grubym tworzy się bardzo dużo polipów, co znacznie zwiększa ryzyko raka jelita grubego)) rozważa się profilaktyczne stosowanie leków, takich jak:
kwas acetylosalicylowy (aspiryna – w małych dawkach)
inhibitory COX-2 (niesteroidowe leki przeciwzapalne – tylko pod kontrolą lekarza)
Warto podkreślić, że profilaktyka pierwotna (zdrowy styl życia) i wtórna (badania przesiewowe) są najskuteczniejszymi metodami walki z rakiem jelita grubego.
Rak jelita grubego rozwija się powoli i można mu skutecznie zapobiec. Wczesne wykrycie – np. poprzez kolonoskopię – ratuje życie. Edukacja, profilaktyka i szybka diagnostyka są kluczem do poprawy rokowań.
Referencje
- NCCN Guidelines®: Colon Cancer (najaktualniejsza wersja — Version 5.2025), https://www.nccn.org/guidelines/guidelines-detail?category=1&id=1428 , data dostępu: 30-03-2026
- NCCN Guidelines®: Rectal Cancer (najaktualniejsza wersja — Version 4.2025), https://www.nccn.org/guidelines/guidelines-detail?category=1&id=1461 , data dostępu: 30-03-2026
- ESMO Clinical Practice Guidelines: Colon Cancer, https://www.esmo.org/guidelines/esmo-clinical-practice-guideline-localised-colon-cancer , data dostępu: 30-03-2026
- ESMO Clinical Practice Guidelines: Rectal Cancer, https://www.annalsofoncology.org/article/S0923-7534%2825%2900731-8/fulltext , data dostępu: 30-03-2026
- ESMO Clinical Practice Guidelines: Metastatic Colorectal Cancer https://www.esmo.org/guidelines/guidelines-by-topic/esmo-clinical-practice-guidelines-gastrointestinal-cancers/clinical-practice-guideline-metastatic-colorectal-cancer , data dostępu: 30-03-2026
- AJCC Cancer Staging Manual, 8th edition (TNM/stadia) https://cancerstaging.org , data dostępu: 30-03-2026
- Fearon ER, Vogelstein B., 1990 — model sekwencji gruczolak–rak: https://pubmed.ncbi.nlm.nih.gov/2032952/ , data dostępu: 30-03-2026
- USPSTF: Colorectal Cancer Screening (najaktualniejsza rekomendacja — 2021, wciąż obowiązuje) https://www.uspreventiveservicestaskforce.org/uspstf/recommendation/colorectal-cancer-screening , data dostępu: 30-03-2026
- ASCO Guidelines – leczenie raka jelita grubego (najbardziej aktualna wytyczna dot. mCRC) https://ascopubs.org/doi/pdfdirect/10.1200/JCO.22.01690 , data dostępu: 30-03-2026
C-ANPROM/PL/NON/0091, 03/2026








